Enlace químico
Enlace iónico, covalente y metálico. Geometría molecular. Fuerzas intermoleculares
 Imagen de Tomislav Jakupec en Pixabay
Imagen de Tomislav Jakupec en Pixabay
Índice
Regla del octeto
La configuración más estable para cualquier átomo es contar con ocho electrones en la capa exterior.
Excepciones
Existen tres excepciones generales a la regla del octeto:
- Moléculas con un número impar de electrones, como el nitrógeno en NO o NO2 (7 e–).
- Moléculas en las que uno o más átomos poseen más de ocho electrones, como el fósforo en PCl5 (10 e–) o el azufre en SF6 (12 e–).
- Moléculas en las que uno o más átomos poseen menos de ocho electrones, como el hidrógeno en H2 (2 e–), el berilio en BeH2 (4 e–) o el boro en BH3, BF3 o BCl3 (6 e–).
Los elementos tenderán a unirse para completar su capa exterior, intercambiando (cediendo/captando $\rightarrow$ enlace iónico) o compartiendo electrones (enlace covalente), y así ganar estabilidad.
Parámetros moleculares
: representa la energía frente a la distancia entre átomos. Según estos se van aproximando, se ponen de manifiesto fuerzas atractivas, pero si se acercan demasiado actúan fuerzas repulsivas. Traducida y adaptada de https://ch301.cm.utexas.edu/section2.php?target=atomic/bonding/covalent-bonding.html.](/media/enlace-quimico-2Bach-quimica/parametros-moleculares.svg)
Energía de enlace
Es la energía desprendida al formar el enlace desde la separación infinita hasta alcanzar la longitud de enlace. Es una medida de la fortaleza de un enlace químico (cuanto mayor sea esta energía, más fuerte será el enlace).
Longitud de enlace
Distancia media entre los núcleos de dos átomos enlazados. Se trata de la distancia óptima en la que la atracción es máxima y la repulsión mínima.
Ángulo de enlace
Ángulo formado por tres átomos enlazados consecutivamente.
Polaridad de enlace
Es la separación de cargas eléctricas a lo largo de un enlace, dando lugar a un momento dipolar eléctrico. La diferencia de electronegatividad, $\Delta \chi$, entre los átomos de un enlace determina su polaridad:

Una molécula será polar si el momento dipolar total (suma vectorial) es distinto de cero.
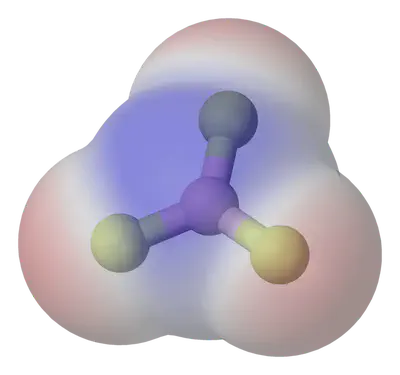
Estudia la polaridad de moléculas con esta excelente simulación:
Enlace iónico
Es un enlace que involucra la atracción electrostática entre iones de signo opuesto. El enlace iónico suele darse entre metales (tienden a ceder electrones, convirtiéndose en cationes) y no metales (tienden a captar electrones, convirtiéndose en aniones). Cada ion tiende a rodearse de un número determinado de iones de signo opuesto (número de coordinación). Se forman así redes cristalinas compactas y neutras con diferentes geometrías según el tipo de iones que las forman.

Adaptada de https://commons.wikimedia.org/wiki/File:Ionic_bonding.svg.

Energía de red o energía reticular $U_\mathrm R$
Es la energía liberada (proceso exotérmico) al formar la red a partir de sus iones en estado gaseoso. Cuanto mayor sea su valor más estable es la red y mayor será el punto de fusión y menor su solubilidad. El cálculo de esta energía se puede hacer mediante el ciclo de Born-Haber (método indirecto) o la ecuación de Born-Landé (método directo).
Ciclo de Born-Haber
Formación de un compuesto iónico a partir de sus elementos.

¿En qué estado están los elementos más comunes de la tabla periódica a temperatura ambiente? Pincha aquí para averiguarlo
| Elemento | Estado a T ambiente | Forma |
|---|---|---|
| Metales (salvo Hg) | Sólido | Atómica |
| Hg | Líquido | Atómica |
| C | Sólido | C (grafito) |
| N | Gas | N2 |
| O | Gas | O2 |
| F | Gas | F2 |
| P | Sólido | P4 (fósforo blanco) |
| S | Sólido | S8 (amarillo) |
| Cl | Gas | Cl2 |
| Se | Sólido | Se (gris) |
| Br | Líquido | Br2 |
| I | Sólido | I2 |
Ecuación de Born-Landé
Permite calcular la energía de red $U_\mathrm R$:
$$ U_\mathrm R = -\frac{N_\mathrm A M z^+ z^- e^2}{4\pi\epsilon_0 r_0}\left(1-\frac{1}{n}\right), $$donde $N_\mathrm A = 6.022\times 10^{23}\thinspace\mathrm{mol^{-1}}$ es la constante de Avogadro; $M$ es la constante de Madelung, relacionada con la geometría del cristal; $z^+$ y $z^-$ son los números de carga del catión y del anión, respectivamente; $e = 1.6\times 10^{-19}\thinspace\mathrm{C}$ es la carga elemental, $\epsilon_0 = 8.85\times 10^{-12}\thinspace\mathrm{C^2N^{-1}m^{-2}}$ es la permitividad eléctrica del vacío; $r_0$ es la distancia al ion más cercano; y $5 < n < 12$ es el exponente de Born (experimental).
Se comprueba que el módulo de la energía de red es:
- Directamente proporcional al producto de las cargas de los iones.
- Inversamente proporcional a la distancia interiónica.
Propiedades de las sustancias iónicas
- Debido a las intensas fuerzas electrostáticas entre los iones, suelen tener temperaturas de fusión y ebullición muy elevadas, por lo que la mayoría son sólidos cristalinos a temperatura ambiente.

🔵 $\rightarrow$ sodio (Na); 🟢 $\rightarrow$ cloro (Cl).
https://freesvg.org/sodium-chloride-crystal
- Ante golpes, el alineamiento de los iones positivos y negativos puede perderse, por lo que son muy frágiles, aunque también muy duros.
- Son solubles en disolventes polares (serán más solubles cuanto menor sea $U_\mathrm R$).
- Fundidos o en disolución, conducen la corriente eléctrica.
Enlace metálico
El enlace metálico es el enlace químico que mantiene unidos a los átomos de un metal entre sí. Surge de la atracción electrostática entre los electrones de conducción y los cationes metálicos.
Modelo del gas electrónico

Teoría de bandas

Puedes aprender más sobre la teoría de bandas y cómo ésta explica la conductividad eléctrica en este excelente artículo.
También os invitamos a leer esta magnífica entrada de Manuel, donde se explica el origen del color del oro haciendo uso de la mecánica cuántica y la teoría de la relatividad.
Este magnífico vídeo de Quantum Made Simple (en inglés) explica la diferencia entre un metal y un aislante:
Propiedades de las sustancias metálicas
- Apariencia brillante.
- Son buenos conductores del calor y de la electricidad.
- Forman aleaciones con otros metales.
- Tienden a ceder (perder) electrones al reaccionar con otras sustancias.
- La mayoría son sólidos a temperatura ambiente (Hg es 💧).
Enlace covalente
Es un enlace químico que implica la compartición de pares de electrones entre átomos. El enlace covalente suele darse entre no metales (tendencia a captar electrones).

Estructuras de Lewis
Se trata de diagramas que muestran la unión entre los átomos de una molécula y los pares solitarios de electrones que pueden existir en la molécula1.
Las estructuras de Lewis muestran cada átomo y su posición en la estructura de la molécula usando su símbolo químico. Se dibujan líneas entre los átomos que están unidos entre sí (se pueden utilizar pares de puntos en lugar de líneas). El exceso de electrones que forman pares solitarios se representan como pares de puntos, y se colocan junto a los átomos.
Pincha aquí para ver cómo construir estructuras de Lewis paso a paso
- Dibujar la molécula de la forma más simétrica posible, colocando los elementos más electronegativos en los extremos.
- Rodear cada elemento del número de electrones de valencia ($N_\mathrm v$).
- Calcular el número máximo de electrones de valencia cumpliendo la regla del octeto ($N_\mathrm{máx}$).
- Calcular el número de electrones enlazados ($N_\mathrm{e} = N_\mathrm{máx} - N_\mathrm{v}$).
- Calcular el número de electrones no enlazados ($N_\mathrm{ne} = N_\mathrm{v} - N_\mathrm{e}$).
Ejemplos
Agua (H2O)

Oxígeno (O2)

Dióxido de carbono (CO2)

Enlace covalente coordinado o dativo
Se trata de enlaces en los que un solo elemento (dador) aporta el par de electrones, el cual es aceptado por otro elemento que tiene un orbital vacío (aceptor). Es un enlace muy común2 y clave para entender el concepto ácido-base de Lewis, en el que el ácido es la especie que acepta el par de electrones (aceptor) y la base la especie que lo cede (dador).

Resonancia
La resonancia es una forma de describir el enlace en ciertas moléculas mediante la combinación de varias estructuras resonantes cuyo conjunto se conoce como un híbrido de resonancia. Es especialmente útil para describir los electrones deslocalizados (enlaces $=$ en distintas posiciones) en ciertas moléculas (O3, SO2) o iones poliatómicos (NO–, NO2–).

Propiedades de las sustancias covalentes moleculares

⚫ $\rightarrow$ carbono (C); 🔴 $\rightarrow$ oxígeno (O); ⚪ $\rightarrow$ hidrógeno (H).
Fuente: https://commons.wikimedia.org/wiki/File:Sucrose_molecule.svg
- Debido a las débiles interacciones entre moléculas covalentes, suelen tener temperaturas de fusión y ebullición bajas (muchos compuestos covalentes son líquidos o gases a temperatura ambiente).
- Son solubles en disolventes polares y apolares (semejante disuelve a semejante).
- En estado sólido son compuestos blandos y frágiles.
- Son malos conductores del calor y de la electricidad.
Propiedades de las sustancias covalentes cristalinas
Las sustancias covalentes cristalinas contienen un gran número de átomos neutros unidos entre sí mediante enlaces covalentes, formando láminas bidimensionales, como el grafito o el grafeno, o estructuras tridimensionales, como el 💎 diamante o el cuarzo.

Fuente: https://commons.wikimedia.org/wiki/File:Graphit_gitter.svg.

- Debido a los fuertes enlaces covalentes entre los átomos, suelen tener temperaturas de fusión y ebullición altas, por lo que son sólidos a temperatura ambiente.
- Son sustancias muy duras aunque frágiles.
- Son insolubles.
- Suelen ser malos conductores (no así el grafito o el grafeno).
Geometría molecular
TRPECV
La Teoría de Repulsión de Pares de Electrones de la Capa de Valencia (TRPECV) se basa en que, como los electrones de valencia se repelen unos a otros, estos tienden a adoptar una disposición espacial que minimiza dicha repulsión.

Ejemplos
Lineal

Trigonal plana

Angular

Tetraédrica

Piramidal trigonal

Bipiramidal trigonal

Balancín

Forma de T

Octaédrica

Piramidal cuadrada

Cuadrada plana

TEV
Según la Teoría del Enlace de Valencia (TEV), un enlace covalente se forma cuando dos orbitales atómicos, cada uno con un electrón desapareado, se solapan de manera eficaz y los electrones de espines opuestos quedan compartidos entre ambos núcleos. Este solapamiento origina un par electrónico enlazante, responsable de la unión entre los átomos:

El número máximo de enlaces que un átomo puede formar depende, por tanto, del número de electrones desapareados que posea en la capa de valencia. En algunos casos, como el del carbono, este número puede aumentarse mediante promoción electrónica, lo que facilita la formación de un mayor número de enlaces equivalentes.
Promoción electrónica
En el marco de la TEV, se asume que un electrón apareado de la capa de valencia puede excitarse a un orbital de mayor energía para aumentar el número de electrones desapareados, que son los que participan en la formación de enlaces. Este proceso no debe interpretarse como una etapa física previa, sino como un recurso conceptual para explicar la capacidad de enlace de átomos como el carbono.
Hibridación
La hibridación es un modelo de la TEV en el que los orbitales atómicos del átomo central se reformulan matemáticamente para dar lugar a orbitales híbridos equivalentes (en energía y geometría) que permiten explicar la orientación espacial y la equivalencia de los enlaces en muchas moléculas.

Pincha aquí para ver en detalle cómo aplicar la TEV
- Se escoge el átomo central.
- Se establece el número de enlaces que debe formar, mediante la estructura de Lewis correspondiente.
- Se comprueba si el número de electrones desapareados disponibles es suficiente para formar los enlaces necesarios. Si no es así, se promocionan los electrones a otros orbitales.
- Se combinan los orbitales atómicos que forman enlaces $\sigma$ (solapamiento frontal) y los que poseen pares de electrones apareados para determinar la hibridación que tendrá lugar en el átomo central.
- Se solapan los orbitales híbridos con los orbitales de los otros átomos con los que forma enlace, teniendo en cuenta la TRPECV para determinar la geometría final de la molécula.
Ejemplos
sp: BeCl2
El berilio no tiene electrones desapareados por lo que se produce promoción electrónica e hibridación para que pueda formar dos enlaces Be—Cl. Cada uno de estos híbridos sp se solapa frontalmente con un orbital p del cloro, formando dos enlaces sigma:


sp2: BF3
El boro solo tiene un electrón desapareado pero necesita tres, por lo que se produce promoción electrónica e hibridación para que pueda formar tres enlaces B—F. Cada uno de estos híbridos sp2 se solapa frontalmente con un orbital p del flúor, formando tres enlaces sigma:


sp3: CH4
El carbono solo tiene dos electrones desapareados pero necesita cuatro, por lo que se produce promoción electrónica e hibridación para que pueda formar cuatro enlaces C—H. Cada uno de estos híbridos sp3 se solapa frontalmente con un orbital s del hidrógeno, formando cuatro enlaces sigma:


Enlaces múltiples
Eteno (CH2=CH2)
Cada carbono necesita formar un enlace doble (con el otro C) y dos enlaces simples (con H), por lo que se necesita promoción electrónica y una hibridación sp2 para tener también un orbital puro p con el que formar un enlace $\pi$ (solapamiento lateral).


Acetileno (CH≡CH)
Cada carbono necesita formar un enlace triple (con el otro C) y un enlace simple (con H), por lo que se necesita promoción electrónica y una hibridación sp para tener dos orbitales puros p con los que formar dos enlaces $\pi$ (solapamiento lateral).


Simulación
Explora las formas moleculares mediante la construcción de moléculas en 3D con la siguiente simulación:
Fuerzas intermoleculares
Las fuerzas intermoleculares son las fuerzas que existen entre las moléculas, incluyendo las fuerzas de atracción o repulsión que actúan entre las moléculas y otros tipos de partículas vecinas, por ejemplo, átomos o iones. Las fuerzas intermoleculares son débiles en relación con las fuerzas intramoleculares (las que mantienen unida una molécula). Son además responsables del estado de agregación, ya que su fortaleza está relacionada con las temperaturas de fusión y ebullición de la sustancia.
Fuerzas de van der Waals

Se pueden dar entre moléculas polares (dipolo-dipolo, más fuertes cuanto mayor sea la polaridad de la molécula), y apolares (llamadas fuerzas de dispersión de London, más fuertes cuanto más grandes y masivas son las moléculas involucradas).
Enlaces de hidrógeno
Son las fuerzas intermoleculares más intensas. Se dan entre moléculas que contienen átomos de hidrógeno unidos a átomos de nitrógeno (N), oxígeno (O) o flúor (F).

Los enlaces de hidrógeno son responsables de:
- Que el agua (H2O) tenga una temperatura de ebullición anormalmente alta (100 °C a presión atmosférica).
- La estructura de proteínas y ácidos nucleicos, como la doble hélice del ADN 🧬.
- La estructura de polímeros.

Participa activamente en la web comentando, dando tu opinión, realizando peticiones, sugerencias...
Discord